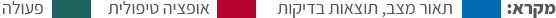צעד 5.4

ביצוע ביופסיה לערמונית.
עדיף ביופסיה פיוז’ן טרנס-פריניאלית
מידע נוסף
מהי ביופסיה לערמונית?
ביופסיה לערמונית הינו תהליך שבו מוציאים דגימות זעירות של רקמה מהערמונית למטופלים שיש חשד שלקו בסרטן הערמונית. אם מתגלות בדגימה אחת, או יותר, רקמה סרטנית אזי זהו האישור הסופי והמוחלט שהנבדק אכן לקה בסרטן הערמונית.
את הדגימות בודקים תחת מיקרוסקופ כדי לגלות:
- האם יש רקמה סרטנית בדגימות שהוצאו.
- מהי האגרסיביות של הרקמה הסרטנית (מדד גליסון).
- באיזה מיקום ממוקמת הרקמה הסרטנית. יש חשיבות רבה לפרמטר זה שכן אין דין רקמה סרטנית הקרובה לדופן הערמונית כדין רקמה סרטנית הנמצאת קרוב למרכז הערמונית. מיקום הרקמה הסרטנית משפיע על ההחלטה מהו דרך הטיפול הטובה ביותר כפונקציה של המיקום.
- כמה אחוזים מתוך כל דגימה היא סרטנית. ככל שאחוזי הרקמה הסרטנית בדגימות יותר גבוהים הדבר מעיד על התפשטות יותר נרחבת של הסרטן.
- מהו הסוג הספציפי של הסרטן בדגימה (הנפוץ ביותר נקרא אדנוקרצינומה). אדנוקרצינומה, Adenocarcinoma – סרטן אשר מתפתח באברים פנימיים מסוימים ויש לו תכונות דומות לבלוטה. (משחרר חומר כלשהו לתוך הגוף). זהו סוג סרטן הערמונית הנפוץ ביותר. לעיתים מתגלים סוגים אחרים של תאים סרטניים שבחלקם אגרסיביים יותר.
- דימום מהרקטום שנפסק בד"כ אחרי כמה ימים
- דם בזרע – בד"כ יש מעט צבע דם (צבע חלודה) בזרע. זה לא סיבה לדאגה מיוחדת ויכול להמשך מספר שבועות לאחר הביופסיה.
- עקבות דם בשתן
- קשיים בהשתנה – תופעה די נדירה שחולפת תוך זמן לא רב לאחר הביופסיה.
- זיהום בדרכי השתן או בערמונית- תופעה די נדירה. יש לפנות לטיפול רופא באמצעות אנטיביוטיקה.
הסבר לגבי הטכניקות השונות לביצוע הביופסיה
ביופסיה לערמונית נעשית ע"מ לאבחן, באופן סופי, חולים בסרטן הערמונית.
הביופסיה שהייתה נהוגה בעבר הינה למעשה "ביופסיה עיוורת". היא נעשית תחת תמונת אולטרה סאונד המתקבלת ממתמר המוכנס לפי הטבעת של הנבדק ומציג, על צג המחשב של הרופא המבצע את מיקום וגבולות הערמונית. למרות זאת, ברוב המקרים תמונת האולטרה סאונד, של הערמונית, אינה מאפשרת להבחין ברקמה הסרטנית וכתוצאה מכך קורים מקרים שהדגימות מהערמונית נלקחות רק מהרקמה הבריאה ולא מהרקמה הנגועה.
כך קורה שמטופל שעבר ביופסיה עיוורת ובאופן שגוי לא נמצאה רקמה סרטנית בערמונית שלו למרות שיש לו סרטן בערמונית.
השגיאות שעלולות לנבוע מביצוע ביופסיה עיוורת הם:
- אי אבחון – בדגימות שהוציא הרופא המבצע לא נמצאה רקמה סרטנית. כל הדגימות שהוצאו היו רק מהרקמה הבריאה, זאת למרות שבפועל קיימת בערמונית רקמה סרטנית.
- אבחון סרטן ברמת אגרסיביות נמוכה – לעיתים נמצאים בדגימות הביופסיה העיוורת תאים סרטניים שנדגמו משולי הרקמה הסרטנית ומתקבלת תוצאה של אגרסיביות נמוכה (מדד גליסון נמוך) ובפועל הרקמה הסרטנית הרבה יותר אגרסיבית (מדד גליסון גבוה). הדבר משתקף בבדיקות הפתולוגיות שנעשית לערמונית לאחר שמוציאים אותה מהגוף באמצעות ניתוח. שגיאה זו יכולה להביא לטיפול שגוי לחולה שזה עתה אובחן.
כיום מקובלת טכניקה משופרת לביצוע הביופסיה הנקראת Fusion biopsy (ביופסיה משולבת) שנעשית תוך שילוב (או היתוך) של הדמיית MRI מוקדמת של הערמונית עם תמונת האולטרה סאונד על הצג של הרופא המבצע את הביופסיה, ובזמן ביצוע הביופסיה, ומאפשרת את הוצאת הדגימות מהערמונית בדיוק מהמקום שבו ישנה רקמה סרטנית כפי שנראית בתמונת ה MRI.
לצורך הזה יש לבצע הדמיית MRI מוקדמת של הערמונית. בהדמיית ה MRI הרופאים שהתמחו בכך, רואים בד"כ היטב את מיקום הרקמה הסרטנית.
ביופסיה בטכניקה הזו מביאה כנראה לרמת גילוי של 85 עד 90 אחוז בעוד שרמת הגילוי של הביופסיה העיוורת הן בסביבת כ – 40 – 35 אחוז. טכניקה זו מביא לשיפור הדיוק באבחון שכן הדגימות בביופסיה פיוזן נלקחות ממרכז הרקמה החשודה כסרטנית ולא משוליה, כפי שעלול לקרות בביופסיה עיוורת.
יתרונות נוספים ל Fusion biopsy –
- מביא להפחתת מספר הביופסיות החוזרות שנעשות בביופסיה עיוורת, שכן השימוש בטכניקה הזו גורם לגילוי הרקמה הסרטנית באופן כמעט ודאי כבר בביופסיה הראשונה.
- מונע מצבים של החמרת המחלה הנגרמת כתוצאה מהזמן שחלף עד לגילויה.
חסרונותיה של ה – Fusion biopsy
- משך הזמן, עד לביצוע הביופסיה בפועל, הוא ארוך מאחר ויש להמתין לתור לביצוע MRI ולאחר מכן להמתין לפיענוח הדמיית הMRI ולאחר מכן יש להמתין לביצוע הביופסיה בפועל. תהליך שיכול לקחת כמה חודשים. מסיבה זו במקרים שה PSA גבוה והתגלתה בערמונית רקמה לא הומגנית/גושים, וברור שהסרטן מפושט בערמונית. במקרה כזה יש דחיפות לאבחון מהיר ולהתחלת הטיפול כדאי לבצע ביופסיה עיוורת הן כדי לחסוך זמן והן משום שסיכויי האבחון מאד גבוהים במצב הזה בביצוע ביופסיה עיוורת.
- מספר המרכזים הרפואיים שבהם מתבצעת ה- Fusion biopsy מצומצם יחסית. עובדה זו גם משפיעה על התארכות משך הזמן עד לביצוע הביופסיה הזו בפועל.
- הדמיית הMRI אינה מגלה ב 100% את הרקמה הסרטנית בערמונית. לעיתים (רחוקות אמנם אבל מקרים כאלו יתכנו) אין הרקמה הסרטנית מתגלה ב MRI. במקרים אלה, ללא גילוי של רקמה סרטנית אין משמעות לבצע את ה- Fusion biopsy.
קיימות שתי טכניקות לביצוע ביופסיה פיוז'ן
הטכניקה הוותיקה יותר הנקראת ביופסיה פיוז'ן טרנס רקטאלית שבמסגרתה מוכנס מתמר אולטרה-סאונד לפי הטבעת של הנבדק ובו מחט המסוגלת לחדור לערמונית מבעד לדופן פי הטבעת ולהוציא דגימה מהערמונית בעיקר מהאזורים החשודים כנגועים כפי שהודגמו בבדיקת ה MRI. היא נעשית בד"כ בהרדמה מקומית.
בגלל המעבר דרך פי הטבעת הסיכון לזיהום בטכניקה זו יוותר גבוה מאשר בטכניקה הטרנס-פריניאלית. ראה כאן
כמו כן לא ניתן להגיע ולהוציא דוגמאות מהחלק הקדמי של הערמונית.
תמונה של ביופסיה טרנס-רקטאלית ניתן לראות בקישור הבא
הביופסיה בטכניקה היותר מתקדמת נקראת ביופסיה פיוז'ן טרנס-פריניאלית. היא מבוצעת במסגרת אשפוז יום כירורגי, נעשית בהרדמה כללית ואורכת כרבע שעה. במסגרת הבדיקה הערמונית נלקחות דגימות ייעודיות מאזורים חשודים כפי שהודגם בהדמיית ה MRI.
לסיכום, לביופסיה טרנס פריניאלית 3 יתרונות חשובים, ביחס לביופסיה טרנס רקטאלית ואלו הם:
- הסיכון לזיהומים נמוך יותר
- היכולת להוציא דגימות מכל נפח הערמונית.
- בניסוי השוואתי נמצא כי יכולת הגילוי של סרטן הערמונית יותר גבוהה בביופסיה הטרנס פריניאלית.
תמונה של ביופסיה טרנס-פריניאלית ניתן לראות בקישור הבא
לסרטון הסבר מצוין, עם ד"ר אילן גיאלצ'ינסקי, על ביופסיה טרנס-פריניאלית – הקש כאן. מומלץ למועמדים לביופסיה להתעקש על ביצוע הביופסיה בשיטה הזו (למעט מקרים שבהם לא ניתן מטעמים שונים לבצע אותה).
הנה כי כן, נראה כי היתרונות של הביופסיה טרנס-פריניאלית מצדיקים את הביצוע שלה למרות הצורך בהרדמה.
הסבר לגבי דרוג גליסון (GLEASON)
דרוג גליסון הינו מדד לחומרה ואגרסיביות של המחלה.
דרוג גליסון נקבע לאחר שדגימות הביופסיה שהוצאו מהערמונית (או לחילופין בדיקה של ערמונית שלמה שהוצאה בניתוח להסרת הערמונית) נבדקות, תחת מיקרוסקופ, ע"י רופא פתולוג המחפש תאים אבנורמליים (לא נורמאליים), תאים שאיבדו את צורתם הטבעית ורקמה שאיבדה את צורתה המקורית. כל תא שנראה סרטני נבדק ומדורג על פי סולם שנקרא GLEASON. מידת האבנורמליות של התא מתבטאת בדרגה שלו בסולם GLEASON. הדרגה הגבוהה ביותר בסולם GLEASON היא 5 והנמוכה ביותר הוא 1. ככל שדרגת ה- GLEASON גבוהה יותר, דרגת החומרה של המחלה גדולה יותר והסרטן אגרסיבי יותר, וכמובן, גדול יותר הסיכון שהסרטן אינו מוגבל רק לערמונית אלא התפשט ממנה והלאה.
דרגת הגליסון הנרשמת בדוח של הפתולוג היא סכום של 2 מספרים (כל אחד בסולם של 1-5).
סה"כ דרגת הגליסון נותנת את המידע לגבי חומרת הגידול.
מהם שני המספרים?
הספרה הראשונה (הנכתבת משמאל) נקבעת ע"י סוג התאים בדגימה המהווים 51% או יותר מהתאים הנצפים בדגימה. הספרה השנייה היא דרגת התאים המצויים בשיעור של לפחות 5% מהדגימה אבל פחות מ- 50%, כלומר בין 5% ל- 49%. סה"כ סכום שני המספרים נותן את דרגת גליסון בסולם של מ- 2 (תקין) ועד 10 (חמור ביותר). למשל: לאדם שיש לו דרגת גליסון של – 7 = 3 + 4 משמעותו שיותר מ- 50% מהתאים בדגימה מראים דרגה 4 ואילו פחות מ- 49% בדגימה מראים דרגה 3.
אדם שיש לו את אותה דרגת גליסון אבל המספרים הם: 7= 4 + 3, מצבו טוב יותר, מפני שיותר מ- 50% מהתאים הם בדרגה 3 והמיעוט הוא בדרגה הגבוהה יותר – דרגה 4.
למעבר לתמונה המדגימה את ההבדלים באופי התאים בסולם גליסון (כאשר בדרגה 1 (בצבע הירוק) המבנה ופיזור של התאים תקין ובצד השני, בדרגה 5 (באדום) האי-סדר והפיזור שלהם מכסימלי) : הקש כאן